|
|
| Vol 27. N°1. 2026 | Enero-Marzo de 2026 |
 |
ARTÍCULOS ORIGINALES
https://doi.org/10.48061/SAN.2026.27.1.8
ASOCIACIÓN ENTRE LOS POLIMORFISMOS rs1801282 EN EL GEN PPARG Y rs7903146 EN TCF7L2 Y PARÁMETROS DE COMPOSICIÓN CORPORAL EN POBLACIÓN ARGENTINA
ASSOCIATION OF THE PPARG rs1801282 AND TCF7L2 rs7903146 POLYMORPHISMS WITH BODY COMPOSITION PARAMETERS IN AN ARGENTINE POPULATION
Luciana Olmedo1, Fernando Javier Luna2, Hernán Dopazo3 y Magalí Pellon Maison4
| 1 |
Instituto de Investigaciones Bioquímicas de La Plata (CONICET- Facultad de Ciencias Médicas, Universidad Nacional de La Plata), Argentina. Programa de Referencia y Biobanco Genómico de la Población Argentina (PoblAr). https://orcid.org/0000-0002-5002-8701 |
| 2 |
Facultad de Ciencias Médicas, Universidad Nacional de La Plata, Argentina. https://orcid.org/0009-0001-5011-2110 |
| 3 |
Laboratorio 2PQ, Instituto de Ecología, Genética y Evolución de Buenos Aires (CONICET - Facultad de Ciencias Exactas y Naturales, Universidad de Buenos Aires), Argentina. Programa de Referencia y Biobanco Genómico de la Población Argentina (PoblAr) https://orcid.org/0000-0001-6125-2357 |
| 4 |
Instituto de Investigaciones Bioquímicas de La Plata (CONICET- Facultad de Ciencias Médicas, Universidad Nacional de La Plata), Argentina. Programa de Referencia y Biobanco Genómico de la Población Argentina (PoblAr). https://orcid.org/0000-0002-7981-5258 |
Correspondencia: Magalí Pellon Maison
E-mail: magalipellon@med.unlp.edu.ar
Presentado: 29/12/25. Aceptado: 23/2/26
RESUMEN
Introducción: La obesidad se caracteriza por una acumulación excesiva de grasa corporal; sin embargo, no todos los individuos presentan comorbilidades metabólicas asociadas. Diversos polimorfismos genéticos se han asociado con este desacople entre adiposidad y riesgo cardiometabólico. En este trabajo se propuso estudiar la asociación entre dos polimorfismos ubicados en los genes PPARG y TCF7L2 y parámetros de composición corporal. Dichas variantes genéticas se han relacionado previamente con el desarrollo de diabetes tipo 2, por lo que se hipotetizó que los alelos de riesgo se asocian con menor adiposidad.
Métodología: Se utilizaron datos provenientes de un estudio transversal analítico realizado en la ciudad de La Plata, Buenos Aires, Argentina. Se obtuvieron genotipos de 157 y 110 voluntarios para los polimorfismos rs1801282 en el gen PPARG y rs7903146 en TCF7L2, respectivamente, mediante qPCR utilizando sondas Taqman. Asimismo, se recopilaron datos sociodemográficos, de actividad física, de ingesta alimentaria y de composición corporal. La composición corporal se evaluó mediante bioimpendaciometría. Se utilizó el análisis de ANCOVA para estudiar las asociaciones entre genotipos y variables de composición corporal.
Resultados: Los portadores del alelo G para rs1801282 en PPARG presentaron un índice de masa corporal (CG+GG= 27,4 vs. CC= 25,6; p=0,011) y un nivel de grasa visceral (CG+GG= 8,24 vs. CC= 7,14; p=0,028) significativamente mayor en comparación con los CC. Adicionalmente, se encontró que el genotipo TT para rs7903146 en TCF7L2 se asoció con un porcentaje de músculo esquelético significativamente menor en comparación con los heterocigotas (TT= 27,1 vs. CT= 31,2; p=0,022). No se hallaron diferencias en los demás parámetros de composición corporal entre genotipos para ambos polimorfismos.
Conclusiones: Los polimorfismos estudiados en PPARG y TCF7L2 se asocian con la composición corporal. Sin embargo, solo el rs1801282 en PPARG contribuiría en el desacople entre adiposidad y riesgo cardiometabólico que se presenta en ciertos fenotipos de obesidad.
Palabras clave: obesidad; índice de masa corporal; composición corporal; PPARG; TCF7L2; Argentina.
ABSTRACT
Introduction: Obesity is characterized by excessive body fat accumulation; however, not all individuals with obesity develop metabolic comorbidities. Several genetic polymorphisms have been linked to this uncoupling between adiposity and cardiometabolic risk. This study aimed to find associations between two polymorphisms located in the PPARG and TCF7L2 genes and body composition parameters. These genetic variants have been previously associated with type 2 diabetes risk; therefore, it was hypothesized that the risk alleles are associated with lower adiposity.
Methods: Data were obtained from an analytical cross-sectional study conducted in the city of La Plata, Buenos Aires, Argentina. Genotypes were obtained from 157 and 110 volunteers for the rs1801282 polymorphism in the PPARG gene and rs7903146 in TCF7L2, respectively, using qPCR with TaqMan probes. Sociodemographic data, physical activity, dietary intake, and body composition were also collected. Body composition was assessed using bioelectrical impedance analysis. ANCOVA was used to evaluate the associations between genotypes and body composition variables.
Results: Carriers of the G allele for rs1801282 in PPARG showed a significantly higher body mass index (CG+GG = 27.4 vs. CC = 25.6; p = 0.011) and a higher visceral fat level (CG+GG = 8.24 vs. CC = 7.14; p = 0.028) compared to CC individuals. Additionally, the TT genotype for rs7903146 in TCF7L2 was associated with a significantly lower percentage of skeletal muscle compared to heterozygotes (TT = 27.1 vs. CT = 31.2; p = 0.022). No differences were observed in the remaining body composition parameters between genotypes for either polymorphism.
Conclusions: The polymorphisms studied in PPARG and TCF7L2 are associated with body composition. However, only rs1801282 in PPARG may contribute to the dissociation between adiposity and cardiometabolic risk observed in certain obesity phenotypes.
Keywords: Obesity; body mass index; body composition; PPARG; TCF7L2; Argentina.
INTRODUCCIÓN
Según la Organización Mundial de la Salud (OMS), la obesidad es una enfermedad crónica compleja, definida por una acumulación excesiva de grasa corporal que puede ser perjudicial para la salud1. Sin embargo, la clasificación de la obesidad como enfermedad aún es controvertida. Es por ello que, con el propósito de abordar las limitaciones del diagnóstico de la obesidad mediante el uso del índice de masa corporal, una comisión de 58 expertos propuso redefinirla distinguiendo entre dos categorías: la "obesidad preclínica", definida como un estado de adiposidad excesiva con función orgánica preservada y con un riesgo variable de desarrollar obesidad clínica y otras enfermedades no transmisibles y la "obesidad clínica" considerada una enfermedad crónica y sistémica, en la que el exceso de adiposidad produce disfunción orgánica, comorbilidades y/o deterioro funcional2.
La evidencia científica actual es concluyente en demostrar que existe una importante variabilidad interindividual en relación con los mecanismos fisiopatológicos que conducen a la acumulación de tejido adiposo, a los riesgos cardiometabólicos asociados a esta y a la eficacia de los tratamientos disponibles3. Por ello, en la actualidad, el diagnóstico, la prevención y el tratamiento de la obesidad se orientan hacia un enfoque basado en la identificación de fenotipos clínicos y biológicos, que permitan una mayor personalización de las intervenciones terapéuticas4,5. Existen distintas dimensiones que permiten identificar estos fenotipos: morfológica, metabólica, funcional, clínica y molecular. Por ejemplo, se ha observado que no todos los individuos con obesidad presentan alteraciones metabólicas, lo que ha llevado a identificar la obesidad metabólicamente saludable (MHO, por sus siglas en inglés), que se caracteriza por un índice de masa corporal elevado y la ausencia de comorbilidades metabólicas, mientras que la obesidad metabólicamente no saludable (MUO) se asocia a disfunción metabólica evidente6-9. A este desacople entre adiposidad y riesgo cardiometabólico, contribuyen diversos factores, tales como la distribución de la grasa corporal, la capacidad de almacenamiento del tejido adiposo, su grado de inflamación, factores hormonales y condicionantes ambientales, entre los que se destacan los patrones alimentarios y el nivel de actividad física.
La variabilidad genética interindividual contribuye de manera significativa al desarrollo de la obesidad, y la identificación de estas variantes genéticas ha sido posible en gran medida gracias a los estudios de asociación de todo el genoma (GWAS, por sus siglas en inglés)10. En este contexto, la genética también desempeña un papel crucial en los mecanismos de desacople entre el aumento de la adiposidad y el riesgo cardiometabólico. Un estudio reciente de metaanálisis11 identificó 62 loci genéticos, en los que el mismo alelo se asoció con mayor adiposidad y menor riesgo cardiovascular y metabólico. Dentro de estos polimorfismos de nucleótido único (SNP, por sus siglas en inglés), destacan los presentes en los genes PPARG (peroxisome proliferator-activated receptor gamma) y TCF7L2 (transcription factor 7-like 2). Se ha demostrado que polimorfismos en estos genes contribuyen al desarrollo de la diabetes de tipo 2. El gen PPARG codifica un receptor nuclear que regula la diferenciación y función de los adipocitos, así como la sensibilidad a la insulina. El polimorfismo rs1801282 C/G conduce a un cambio de prolina por alanina en la posición 12 de la proteína (Pro12Ala) y el alelo Ala se ha asociado de manera robusta con un efecto protector para el desarrollo de insulino-resistencia y diabetes de tipo 212, aunque sus efectos se encuentran modulados por factores ambientales como la dieta y el nivel de actividad física. Por otro lado, el gen TCF7L2 está involucrado en la vía de señalización Wnt/β-catenina, crucial para la homeostasis de la glucosa y la función de las células β pancreáticas. El alelo T del polimorfismo rs7903146 C/T en TCF7L2 es la variante genética con mayor tamaño de efecto para el desarrollo de diabetes de tipo 2, hallazgo que se ha replicado en distintas poblaciones13. Aunque el efecto de estos polimorfismos en el desarrollo de la diabetes de tipo 2 se ha documentado ampliamente, su contribución a la variabilidad de la composición corporal resulta menos consistente. Por ello, el objetivo de este trabajo fue estudiar la asociación de estos polimorfismos con parámetros de composición corporal, bajo la hipótesis de que los alelos de riesgo para diabetes de tipo 2 se asocian con menor adiposidad, actuando como variantes genéticas de desacople entre adiposidad y riesgo cardiometabólico.
METODOLOGÍA
Diseño del estudio y participantes
Participaron del estudio 173 adultos de ambos sexos con edades comprendidas entre 19 y 60 años, previamente reclutados en un estudio transversal analítico14 que se llevó a cabo en la ciudad de La Plata y sus alrededores. Se excluyó a embarazadas, lactantes y a individuos que habían tenido cambios en su alimentación en los últimos dos años. Los participantes fueron reclutados mediante un muestreo voluntario y no probabilístico, y la totalidad de ellos firmaron el consentimiento informado previamente a su participación. Brevemente, la población estudiada presentó una edad media de 33,5 años con un 43,9% de individuos de sexo femenino y un 56,1% de sexo masculino. A su vez, del total de participantes, un 38,6% completó el nivel educativo universitario o terciario, un 43,3% el secundario, y un 18,1% el primario. La media del índice de masa corporal (IMC) de esta muestra fue de 25,6 kg/m2 con un mínimo de 18,1 kg/m2 y un máximo de 36,1 kg/m2. De esta población se obtuvieron los genotipos para 157 voluntarios en el caso de la variante rs1801282 C/G localizada en el gen PPARG, y para 110 participantes para la variante rs7903146 C/T en TCF7L2. Los datos sociodemográficos, de actividad física, de composición corporal, de ingesta alimentaria y la muestra de saliva para la genotipificación fueron recolectados mediante una entrevista realizada por Licenciados en Nutrición entrenados para ello en el Instituto de Investigaciones Bioquímicas de La Plata (INIBIOLP), localizado en la Facultad de Ciencias Médicas de la Universidad Nacional de La Plata. El protocolo de investigación fue aprobado por el Comité de Bioética de la Facultad de Ciencias Médicas de la Universidad Nacional de La Plata (COBIMED) bajo el protocolo n°46/18.
Tamaño muestral
Para el cálculo del poder estadístico se utilizó el programa G*power 3.1.9.715. Con un poder estadístico del 80% y un nivel de significancia de 0,05, la muestra de 157 voluntarios (variante genética en PPARG) que se analizó mediante un modelo genético dominante (2 grupos) permite detectar asociaciones entre las variables de composición corporal y el genotipo con un tamaño de efecto entre chico y mediano (f= 0,23) de acuerdo a la clasificación de Cohen16, mientras que la muestra de 110 individuos (polimorfismo en TCF7L2) que se analizó bajo un modelo genético codominante (3 grupos) permite detectar asociaciones con un tamaño de efecto entre mediano y grande (f= 0,30).
Variables
Se incluyó información sociodemográfica, de actividad física, de composición corporal, de ingesta alimentaria, y genética de los voluntarios. Las variables sociodemográficas comprendieron edad, sexo y nivel educativo. Los niveles de actividad física se determinaron según los criterios de la OMS17. Se consideró que los individuos eran físicamente activos si realizaban al menos 150 minutos por semana de actividad física aeróbica de intensidad moderada o 75 minutos por semana de actividad física aeróbica de alta intensidad, o una combinación equivalente de ambas.
Las variables antropométricas fueron peso, talla, índice de masa corporal (IMC), % de masa grasa, % de músculo esquelético y nivel de grasa visceral. La talla fue registrada por duplicado al último 0,1 cm completo utilizando un tallímetro de pared Seca 206, y se calculó el promedio de ambas mediciones. El peso y los parámetros de composición corporal se midieron por única vez utilizando una balanza de bioimpedancia Omron HBF514c. Para ello, los participantes se encontraron en ayunas, sin medias ni zapatos y con ropa liviana.
Los datos de ingesta alimentaria se recolectaron mediante un cuestionario de frecuencia alimentaria previamente validado en la misma población, denominado CFA-UP18, e incluyeron la ingesta habitual diaria de energía total y nutrientes. Específicamente se evaluó la ingesta de carbohidratos, proteínas, grasas totales, azúcares totales, azúcares libres, ácidos grasos saturados, ácidos grasos monoinsaturados y ácidos grasos poliinsaturados como % de la energía total, el consumo de fibra en gramos por día y la ingesta de colesterol en mg por día.
En relación con los datos genéticos, se obtuvieron los genotipos de los participantes para las variantes genéticas rs1801282 C/G, localizada en el gen PPARG y rs7903146 C/T, localizada en el gen TCF7L2. Los genotipos se obtuvieron por extracción del ADN a través de muestras de saliva, mediante PCR en tiempo real utilizando sondas de fluorescencia Taqman.
Análisis estadístico
A partir de los datos recopilados, se creó una base de datos utilizando el paquete estadístico SPSS, versión 25.0 para Windows19. Se estimaron las frecuencias alélicas y genotípicas de los distintos SNPs, y mediante el test Chi2 se determinó la existencia o no de diferencias significativas entre las frecuencias alélicas de la muestra estudiada y de la población americana y europea del proyecto 1000 genomas20.
Las asociaciones entre los genotipos y los indicadores antropométricos IMC, % de masa grasa, % de músculo esquelético y nivel de grasa visceral se analizaron mediante ANCOVA, ajustando por las variables de confusión edad, sexo, nivel de actividad física y nivel educativo. Dichos modelos se realizaron utilizando el modelo genético dominante para la variante genética localizada en el gen PPARG (portadores del alelo de riesgo vs. homocigotas más frecuentes) y el modelo genético codominante (homocigotas del alelo de riesgo vs. heterocigotas vs. homocigotas más frecuentes) para la variante genética ubicada en el gen TCF7L2.
Adicionalmente, se estudiaron las asociaciones entre genotipos para ambas variantes genéticas y la ingesta de energía total y nutrientes. Para establecer las asociaciones entre el alelo G para el polimorfismo en PPARG o el alelo T para la variante genética en TCF7L2 y la ingesta de energía total nutrientes se utilizaron modelos lineales generales, en los cuales se excluyeron previamente los datos atípicos (Modelo 1). En el Modelo 2 se realizó un ajuste por las variables de confusión edad, sexo, nivel educativo y nivel de actividad física, mientras que en el Modelo 3 se incluyó como variable de confusión adicional al IMC. A su vez, se obtuvieron las medias estimadas para los portadores del alelo G (CG+GG) y para los individuos CC para la variante genética en PPARG, y para cada uno de los genotipos (CC, CT Y TT) en el caso del polimorfismo en TCF7L2. En este último, las medias estimadas se compararon por medio del análisis post-hoc de Bonferroni.
RESULTADOS
Frecuencias alélicas y genotípicas: las frecuencias genotípicas del polimorfismo rs7903146 en TCF7L2 fueron CC= 50%, CT= 42,7 % y TT= 7,3 %. A partir de estos resultados, se calcularon las frecuencias alélicas: T= 29 % y C = 71 %. Las frecuencias genotípicas observadas se compararon con las esperadas bajo el modelo de Hardy-Weinberg. No se encontraron diferencias estadísticamente significativas entre los valores observados y esperados, por lo que la población se encuentra en equilibrio (HWE Chi2= 0,20, p= 0,66). Además, se compararon las frecuencias alélicas con las reportadas en el proyecto 1000 Genomas y no se hallaron diferencias estadísticamente significativas entre las encontradas en la población en estudio y las halladas en población europea yamericana. Por otra parte, las frecuencias genotípicas del polimorfismo rs1801282 en PPARG fueron CC= 78,3%, CG= 21,0% y GG= 0,7%, y las frecuencias alélicas C= 89% y G= 11%. En este caso también se verificó el equilibrio de Hardy-Weinberg (HWE Chi2= 0,31, p= 0,58) y las frecuencias no fueron diferentes a las encontradas en el proyecto 1000 Genomas en poblaciones americanas y europeas.
Asociación entre los polimorfismos rs7903146 en TCF7L2 y rs1801282 en PPARG con parámetros de composición corporal: la Figura 1 muestra el índice de masa corporal, el porcentaje de masa grasa, el porcentaje de músculo esquelético y el nivel de grasa visceral para los distintos genotipos en el locus polimórfico en PPARG. Los resultados muestran que los portadores del alelo G (CG+GG) tuvieron un índice de masa corporal y un nivel de grasa visceral 7 % y 15,4 % mayor al de los homocigotas CC, respectivamente. Por otra parte, no se encontraron diferencias en los porcentajes de masa grasa y músculo esquelético. En la Figura 2 se muestran los resultados obtenidos para el polimorfismo rs7903146 en el gen TCF7L2. En este caso, se observaron diferencias estadísticamente significativas en el porcentaje de músculo esquelético, siendo el valor para los homocigotas TT 13,1% menor que para los heterocigotas.
| Figura 1: Variables de composición corporal para adultos (n=157) residentes en la ciudad de La Plata, de acuerdo a los genotipos para el polimorfismo rs1801282 C/G ubicado en el gen PPARG
|
| |
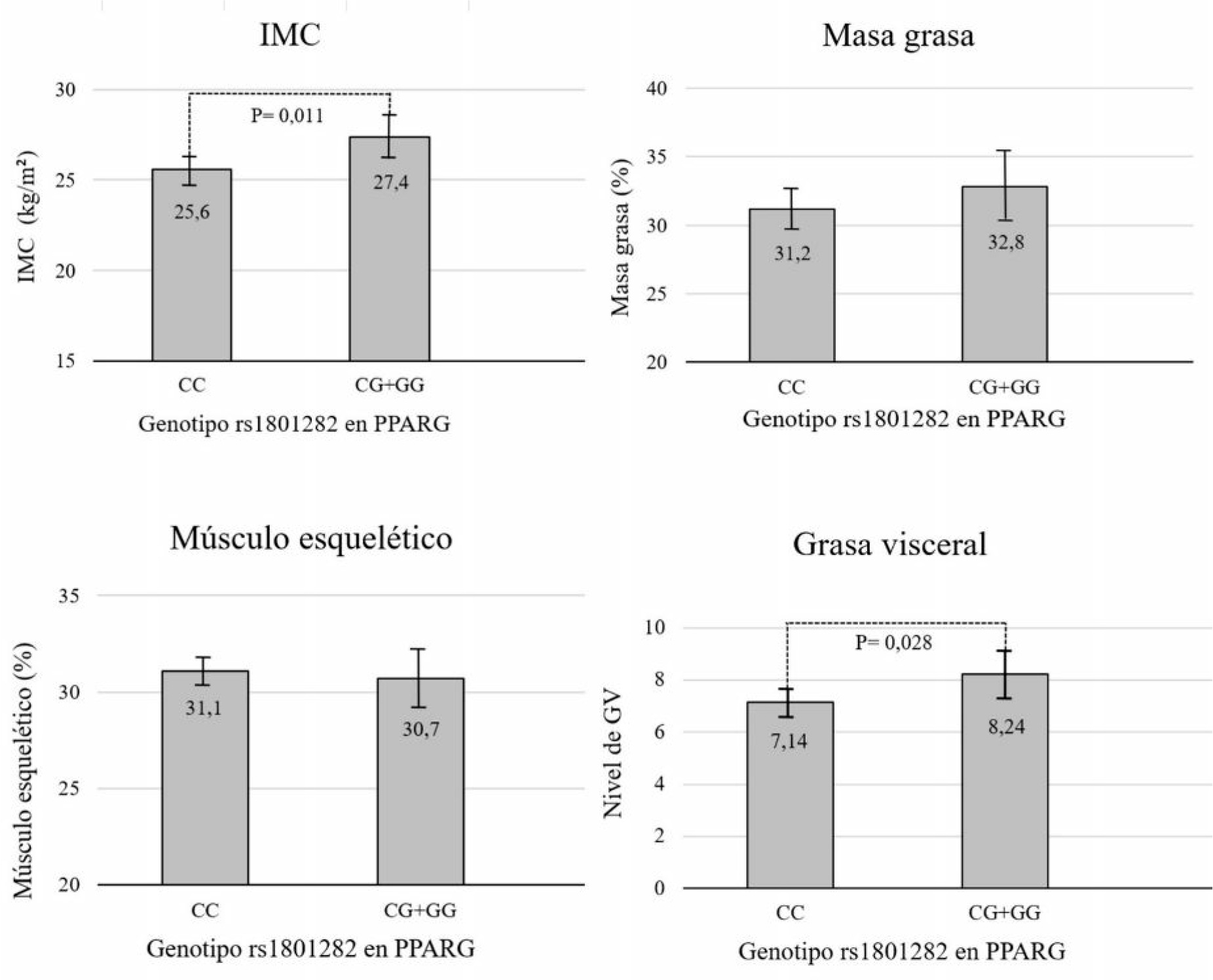 |
Las medias estimadas de Índice de Masa Corporal (IMC), masa grasa, músculo esquelético y nivel de grasa visceral (GV) de acuerdo al genotipo dominante para rs1801282 C/G ubicado en el gen PPARG (CC, n= 123; CG+GG, n=34) se obtuvieron mediante el análisis de ANCOVA, ajustando por edad, sexo, nivel de actividad física y nivel educativo. El nivel de significancia se estableció en 0,05.
| Figura 2: Variables de composición corporal para adultos (n=110) residentes en la ciudad de La Plata, de acuerdo a los genotipos para el polimorfismo rs7903146 C/T ubicado en el gen TCF7L2
|
| |
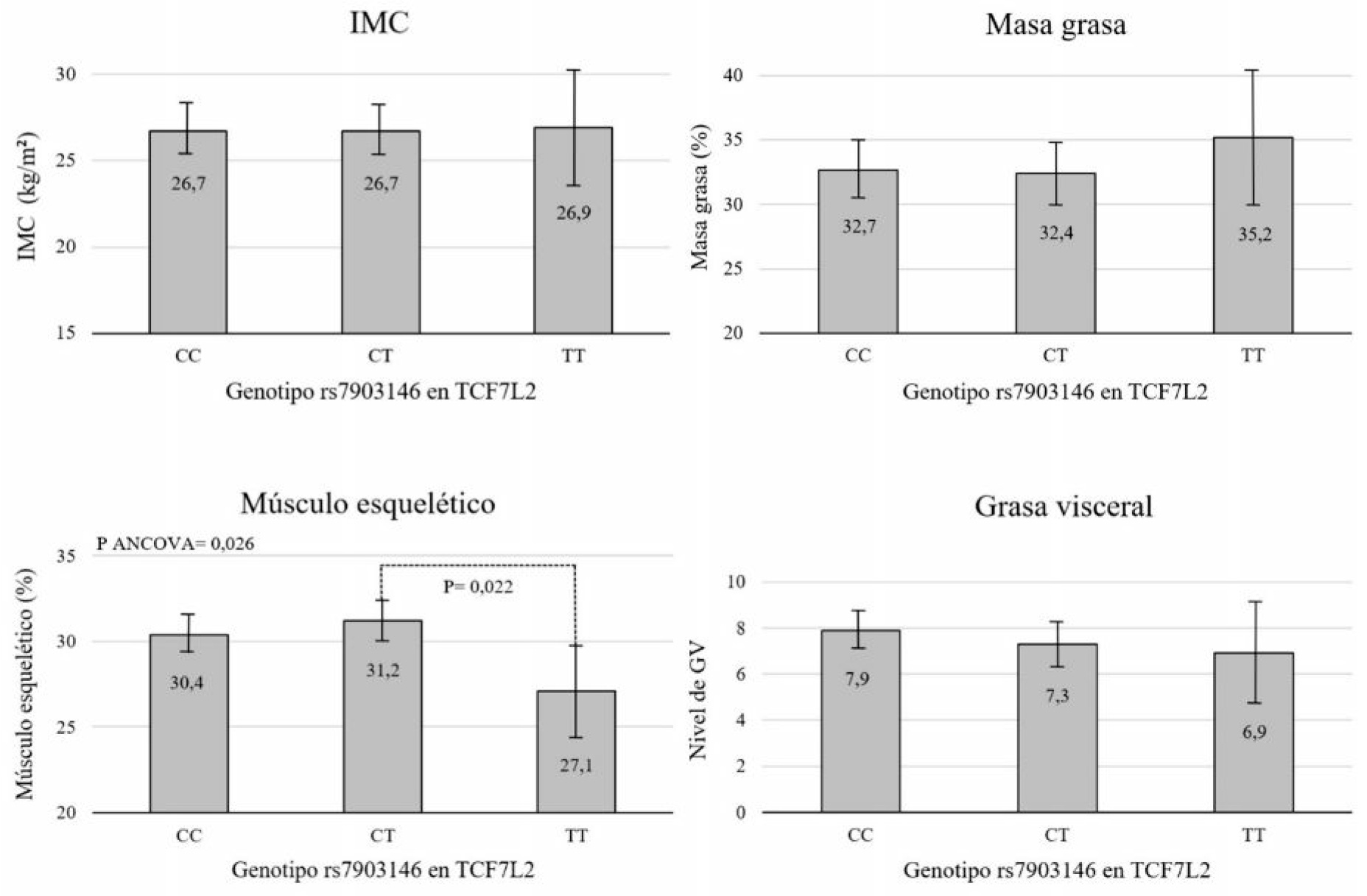 |
Las medias estimadas de Índice de Masa Corporal (IMC), masa grasa, músculo esquelético y nivel de grasa visceral (GV) de acuerdo al genotipo dominante para rs7903146 C/T ubicado en el gen TCF7L2 (CC, n= 55; CT, n=47; TT, n=8) se obtuvieron mediante el análisis de ANCOVA, ajustando por edad, sexo, nivel de actividad física y nivel educativo. Las comparaciones post-hoc se realizaron utilizando Bonferroni. El nivel de significancia se estableció en 0,05.
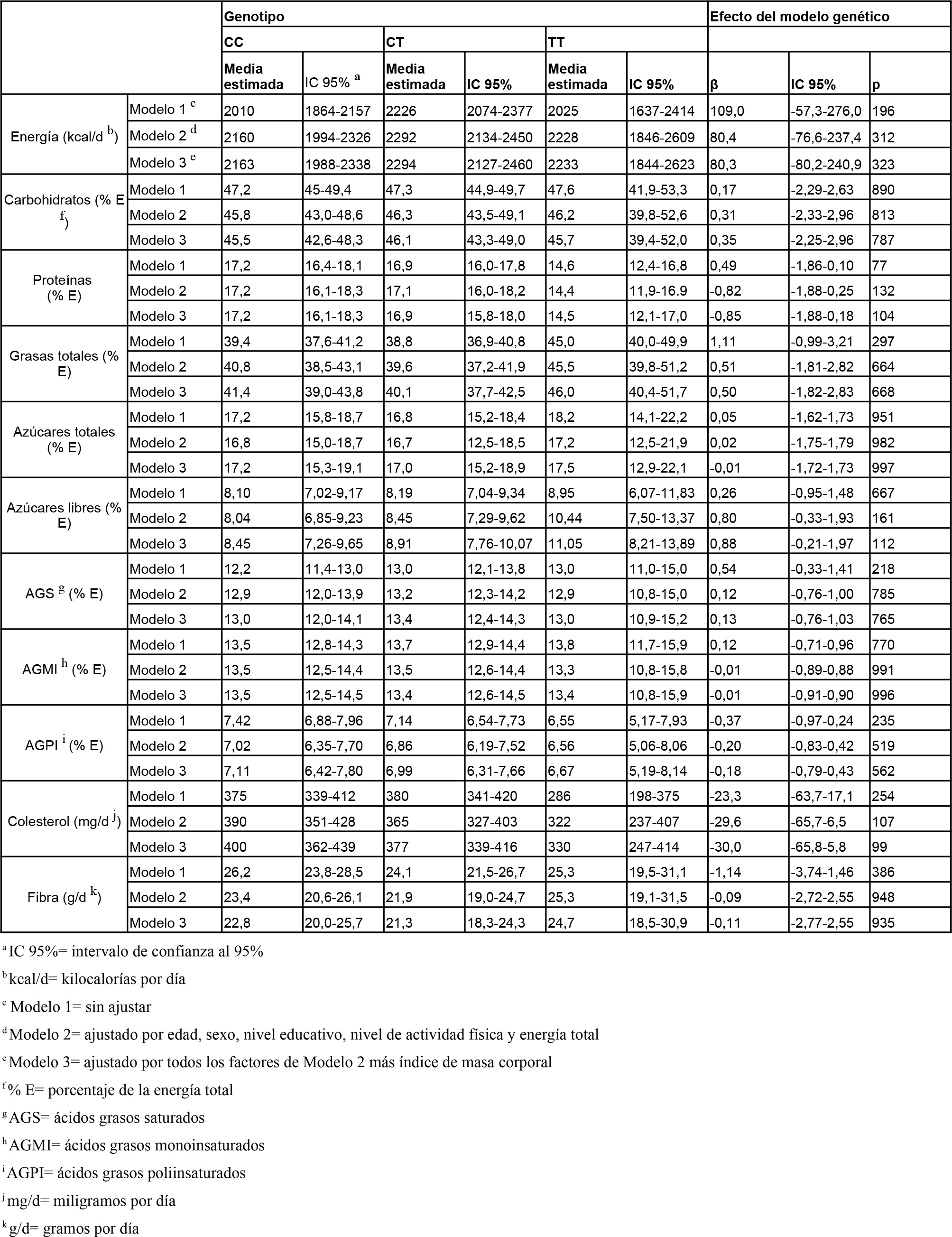
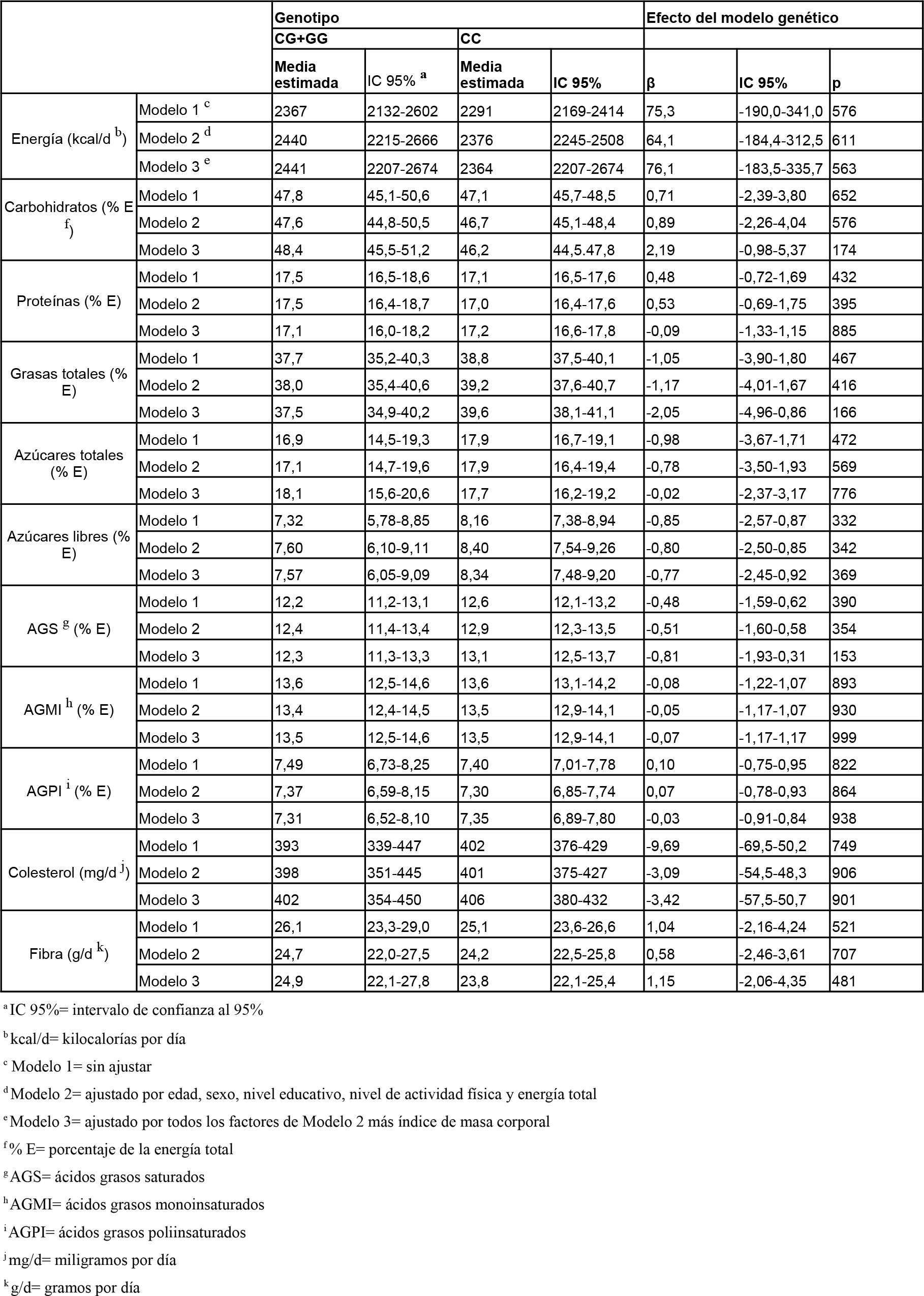
Asociación entre los polimorfismos rs7903146 en TCF7L2 y rs1801282 en PPARG con la ingesta alimentaria: las tablas 1 y 2 muestran los datos de ingesta de energía y de nutrientes en función de los genotipos para los distintos polimorfismos analizados. No se observaron diferencias estadísticamente significativas para ninguno de los nutrientes analizados.
| Tabla 1: Ingesta de energía total y de macronutrientes según genotipos en TCF7L2 (rs7903146 C/T)
|
| |
 |
| Tabla 2: Ingesta de energía total y de macronutrientes según genotipos en PPARG (rs1801282 C/G)
|
| |
 |
DISCUSIÓN
Los estudios de asociación de todo el genoma (GWAS) han permitido identificar polimorfismos genéticos asociados al índice de masa corporal y otras variables de composición corporal. En el año 2007, dos GWAS identificaron polimorfismos en el primer intrón del gen FTO (fat mass and obesity related gene), como los más fuertemente asociados y con mayor tamaño de efecto sobre el índice de masa corporal21,22, hallazgo que luego se replicó en poblaciones de distintas ancestrías23-25. En estudios previos, encontramos que en población adulta argentina, cada alelo de riesgo A del polimorfismo rs9939609 en el gen FTO, incrementó el índice de masa corporal en 1.4 kg/m2 ([0.50-2.2], p = 0.002), el porcentaje de masa grasa en 2.5 % ([0.8-4.2], p = 0.004) y el nivel de grasa visceral en 0,7 unidades arbitrarias ([0.09-1.4], p = 0.026) y disminuyó el porcentaje de músculo esquelético en 1.5 % ([-2.5, 0.6], p = 0.009)26. Asimismo, en concordancia con estudios previos, encontramos que el polimorfismo rs9939609 en el gen FTO contribuyó a la variabilidad de la ingesta alimentaria, siendo los portadores del alelo A más adherentes al patrón alimentario occidental, con una mayor ingesta de grasas totales y grasas saturadas 14. En este trabajo, se propuso extender los hallazgos obtenidos para esta población, al efecto de dos polimorfismos fuertemente asociados al desarrollo de diabetes de tipo 2, bajo la hipótesis de que los alelos de riesgo para diabetes se asocian con menor adiposidad. En este contexto, se encontró que el alelo Ala del polimorfismo rs1801282 en PPARG, se asoció con un mayor índice de masa corporal, a expensas de un aumento del nivel de grasa visceral. Es decir que el alelo protector para diabetes de tipo 2, se asoció con mayor adiposidad central. Estos resultados concuerdan con los obtenidos en un metaanálisis que incluyó datos de 75 estudios independientes con 49.092 individuos27. En relación con la composición corporal, el estudio familiar de Quebec28 también encontró que los portadores del alelo Ala mostraron un mayor índice de masa corporal, circunferencia de cintura, masa grasa, grasa subcutánea y grasa visceral en comparación con los homocigotas Pro/Pro. Es importante destacar que la evidencia científica sugiere que el efecto de este polimorfismo sobre los parámetros de composición corporal está modulado por la dieta29-31.
Por otra parte, el alelo T del polimorfismo rs7903146 en TCF7L2 se ha asociado en estudios previos con un menor índice de masa corporal, incluso en poblaciones latinas residentes en los Estados Unidos32,33. A pesar de que en nuestra población de estudio se replicaron los efectos de los polimorfismos rs9939609 del gen FTO 26 y rs1801282 en PPARG sobre el índice de masa corporal, en el caso de rs7903146 en TCF7L2 no se encontró un efecto protector del alelo T sobre el parámetro ni en los otros asociados a adiposidad. Por el contrario, se observó que el alelo T se asoció con un menor porcentaje de masa muscular. Según nuestro conocimiento, este hallazgo no ha sido reportado previamente en la literatura.
En el presente estudio, los polimorfismos en PPARG y TCF7L2 se asociaron con variables de composición corporal, en concordancia con lo reportado previamente en la literatura. Sin embargo, los mecanismos biológicos que subyacen a estas asociaciones no están completamente dilucidados. A diferencia de lo observado para variantes en FTO, cuya relación con la adiposidad se ha vinculado a modificaciones en los niveles de saciedad y la ingesta de macronutrientes14,26, en este trabajo los polimorfismos en PPARG y TCF7L2 no se asociaron con variaciones en la ingesta de energía y nutrientes, tal como era esperable considerando sus funciones metabólicas. En este contexto, futuros estudios que integren aproximaciones funcionales podrían contribuir a una mejor comprensión del rol de estos polimorfismos en la variabilidad de la composición corporal y los mecanismos de desacople con el riesgo cardiometabólico.
Entre las limitaciones de este estudio debe considerarse su diseño observacional que impide establecer relaciones causales y el tamaño muestral relativamente pequeño, que podría haber limitado la potencia estadística para detectar asociaciones de menor magnitud. No obstante, el estudio presenta fortalezas, entre ellas la aplicación de protocolos estandarizados, la evaluación conjunta de la composición corporal, la ingesta alimentaria y las variantes genéticas de interés biológico, así como la contribución de datos originales en una población poco caracterizada desde el punto de vista nutrigenético.
CONCLUSIONES
Teniendo en cuenta que de acuerdo con los resultados obtenidos en el presente estudio, el alelo protector Ala (G) para el polimorfismo rs1801282 en PPARG, se asocia con un mayor índice de masa corporal y un mayor nivel de grasa visceral, es decir, con una mayor adiposidad central, y que el alelo de riesgo T para el rs7903146 en TCF7L2 se asocia con un menor porcentaje de músculo esquelético, se concluye que las variantes genéticas estudiadas en PPARG y TCF7L2 se asocian con la composición corporal. Sin embargo, solo la variante genética ubicada en el gen PPARG contribuiría en el desacople entre adiposidad y riesgo cardiometabólico generado en ciertos fenotipos de obesidad. Estos hallazgos resultan relevantes para profundizar en el conocimiento de los distintos fenotipos clínicos y biológicos relacionados a obesidad identificados hasta el momento, y para dar lugar en última instancia a intervenciones terapéuticas con un mayor grado de personalización.
Financiamiento
Este trabajo fue parcialmente financiado por La Sociedad Argentina de Nutrición ("Interacción entre variantes genéticas y variables alimentarias sobre indicadores antropométricos de riesgo cardiovascular", primer Premio del Subsidio de Investigación Científica 2023) y por la Universidad Nacional de La Plata (código del proyecto M246, año 2023).
Conflictos de interés
Los autores declaran no tener conflictos de interés.
REFERENCIAS
- World Health Organization (WHO). Obesity and Overweight. (2025). https://www.who.int/news-room/fact-sheets/detail/obesity-and-overweight. Recuperado el 10 de diciembre de 2025
- Rubino F, Cummings DE, Eckel RH, et al. Definition and diagnostic criteria of clinical obesity. Lancet Diabetes Endocrinol. 2025;13(3):221-262. doi:10.1016/S2213-8587(24)00316-4
- Loos RJF. Genetic causes of obesity: mapping a path forward. Trends Mol Med. 2025;31(4):319-325. doi:10.1016/j.molmed.2025.02.002
- Acosta A, Camilleri M, Abu Dayyeh B, et al. Selection of Antiobesity Medications Based on Phenotypes Enhances Weight Loss: A Pragmatic Trial in an Obesity Clinic. Obesity. 2021;29(4):662-671. doi:10.1002/oby.23120
- Zandvakili I, Pulaski M, Pickett-Blakely O. A phenotypic approach to obesity treatment. Nutr Clin Pract. 2023;38(5):959-975. doi:10.1002/ncp.11013
- Primeau V, Coderre L, Karelis AD, et al. Characterizing the profile of obese patients who are metabolically healthy. Int J Obes. 2011;35(7):971–981. doi:10.1038/ijo.2010.216
- Blüher M. Metabolically healthy obesity. Endocr Rev. 2020;41(3):bnaa004. doi:10.1210/endrev/bnaa004
- Karelis AD, Messier V, Brochu M, Rabasa-Lhoret R. Metabolically healthy but obese women: Effect of an energy-restricted diet. Diabetologia. 2008;51(9):1752-1754. doi:10.1007/s00125-008-1038-4
- Sims EAH. Are there persons who are obese, but metabolically healthy? Metabolism. 2001;50(12):1499-1504. doi:10.1053/meta.2001.27213
- Loos RJF, Yeo GSH. The genetics of obesity: from discovery to biology. Nat Rev Genet. 2022;23(2):120-133. doi:10.1038/s41576-021-00414-z
- Huang LO, Rauch A, Mazzaferro E, et al. Genome-wide discovery of genetic loci that uncouple excess adiposity from its comorbidities. Nat Metab. 2021;3(2):228-243. doi:10.1038/s42255-021-00346-2
- Sarhangi N, Sharifi F, Hashemian L, et al. PPARG (Pro12Ala) genetic variant and risk of T2DM: a systematic review and meta-analysis. Sci Rep. 2020;10(1):12764. doi:10.1038/s41598-020-69363-7
- Cauchi S, El Achhab Y, Choquet H, et al. TCF7L2 is reproducibly associated with type 2 diabetes in various ethnic groups: A global meta-analysis. J Mol Med. 2007;85(7):777–782. doi:10.1007/s00109-007-0203-4
- Olmedo L, Luna FJ, Zubrzycki J, Dopazo H, Pellon-Maison M. Associations Between rs9939609 FTO Polymorphism With Nutrient and Food Intake and Adherence to Dietary Patterns in an Urban Argentinian Population. J Acad Nutr Diet. 2024;124(7):874-882. doi:10.1016/j.jand.2024.01.001
- Faul F, Erdfelder E, Buchner A, Lang A. Statistical power analyses using G*Power 3.1: Tests for correlation and regression analyses. Behav Res Methods. 2009;41(4):1149-1160. doi:10.3758/BRM.41.4.1149
- Cohen J. A power primer. Psychol Bull. 1992;112(1):155-159. doi:10.1037//0033-2909.112.1.155
- Organización Mundial de la Salud (OMS). Directrices de la OMS sobre actividad física y hábitos sedentarios: de un vistazo (2020). https://apps.who.int/iris/rest/bitstreams/1318324/retrieve. Recuperado el 10 deciembre de 2025
- Olmedo L, Henning M, García S, Pellon Maison M. Validación de un cuestionario de frecuencia alimentaria para estimar la ingesta de azúcares libres y alimentos ultraprocesados en población argentina. Rev Española Nutr Humana Y Dietética. 2022;26(2):137-146. doi:10.14306/renhyd.26.2.1565
- IBM SPSS Statistics for Windows (2017). Version 25.0. https://www.ibm.com/es-es/spss.
- Auton A, Abecasis GR, Altshuler DM, et al. A global reference for human genetic variation. Nature.Nature Publishing Group. 2015;526(7571):68-74. doi:10.1038/nature15393
- Frayling TM, Timpson NJ, Weedon MN, et al. A common variant in the FTO gene is associated with body mass index and predisposes to childhood and adult obesity. Science (80- ). 2007;316(5826):889-894. doi:10.1126/science.1141634
- Scuteri A, Sanna S, Chen WM, et al. Genome-wide association scan shows genetic variants in the FTO gene are associated with obesity-related traits. PLoS Genet. 2007;3(7):1200-1210. doi:10.1371/journal.pgen.0030115
- Loos RJF, Lindgren CM, Li S, et al. Common variants near MC4R are associated with fat mass, weight and risk of obesity. Nat Genet. 2008;40(6):768-775. doi:10.1038/ng.140
- Wing MR, Ziegler J, Langefeld CD, et al. Analysis of FTO gene variants with measures of obesity and glucose homeostasis in the IRAS Family Study. Hum Genet. 2009;125(5-6):615–626. doi:10.1007/s00439-009-0656-3
- Hotta K, Nakata Y, Matsuo T, et al. Variations in the FTO gene are associated with severe obesity in the Japanese. J Hum Genet. 2008;53(6):546–553. doi:10.1007/s10038-008-0283-1
- Olmedo L, Luna FJ, Dopazo H, Pellon-Maison M. Protein and total sugars intake modulate the rs9939609 single nucleotide polymorphism effect at the fat mass and obesity-associated gene on body composition. Clin Nutr ESPEN. 2025;68:359-367. doi:10.1016/j.clnesp.2025.05.032
- Galbete C, Toledo E, Martínez-González MA, Martínez JA, Guillén-Grima F, Marti A. Pro12Ala variant of the PPARG2 gene increases body mass index: An updated meta-analysis encompassing 49,092 subjects. Obesity. 2013;21(7):1486-1495. doi:10.1002/oby.20150
- Robitaille J, Després JP, Pérusse L, Vohl MC. The PPAR-gamma P12A polymorphism modulates the relationship between dietary fat intake and components of the metabolic syndrome: Results from the Québec Family Study. Clin Genet. 2003;63(2):109-116. doi:10.1034/j.1399-0004.2003.00026.x
- Lamri A, Abi Khalil C, Jaziri R, et al. Dietary fat intake and polymorphisms at the PPARG locus modulate BMI and type 2 diabetes risk in the D.E.S.I.R. prospective study. Int J Obes. 2012;36(2):218-224. doi:10.1038/ijo.2011.91
- Luan J, Browne PO, Harding AH, et al. Evidence for gene-nutrient interaction at the PPARγ locus. Diabetes. 2001;50(3):686-689. doi:10.2337/diabetes.50.3.686
- Garaulet M, Smith CE, Hernández-González T, Lee YC, Ordovás JM. PPARγ Pro12Ala interacts with fat intake for obesity and weight loss in a behavioural treatment based on the Mediterranean diet. Mol Nutr Food Res. 2011;55(12):1771-1779. doi:10.1002/mnfr.201100437
- Cauchi S, Choquet H, Gutiérrez-Aguilar R, et al. Effects of TCF7L2 polymorphisms on obesity in European populations. Obesity. 2008;16(2):476-482. doi:10.1038/oby.2007.77
- Fernández-Rhodes L, Howard AG, Graff M, et al. Complex patterns of direct and indirect association between the transcription Factor-7 like 2 gene, body mass index and type 2 diabetes diagnosis in adulthood in the Hispanic Community Health Study/Study of Latinos. BMC Obes. 2018;5(1). doi:10.1186/s40608-018-0200-x
|
|

