|
|
| Vol 26. N°4. 2025 | Octubre-Diciembre de 2025 |
 |
REVISIÓN
https://doi.org/10.48061/SAN.2025.26.4.293
MICROBIOTA INTESTINAL, LACTOSA Y ABORDAJE NUTRICIONAL EN NIÑOS CON FENILCETONURIA
INTESTINAL MICROBIOTA, LACTOSE, AND NUTRITIONAL APPROACH IN CHILDREN WITH PHENYLKETONURIA
Adriana Becerra1, Inés Bertero2, Verónica Bindi3, Mariana Inés Núñez4, Mercedes Salerno5, Jacqueline Schuldberg6, María Gabriela Valle7, Gabriel Vinderola8
| 1 |
Hospital de Niños de la Santísima Trinidad, Córdoba, Argentina. https://orcid.org/0009-0002-4710-8062 |
| 2 |
Hospital de Niños de la Santísima Trinidad, Córdoba, Argentina. https://orcid.org/0009-0001-0506-5183 |
| 3 |
Hospital Juan P. Garrahan, Ciudad Autónoma de Buenos Aires, Argentina. https://orcid.org/0000-0002-5872-199X |
| 4 |
Hospital Interzonal de Agudos Especializado en Pediatría Sor María Ludovica de La Plata, Buenos Aires, Argentina. https://orcid.org/0000-0001-5003-7651 |
| 5 |
Hospital Interzonal de Agudos Especializado en Pediatría Sor María Ludovica de La Plata, Buenos Aires, Argentina. https://orcid.org/0000-0001-8710-9620 |
| 6 |
Centro Médico del Niño y la Mujer y Medical & Nutrition Science, Danone Specialized Nutrition. Ciudad Autónoma de Buenos Aires, Argentina. https://orcid.org/0009-0006-4288-116X |
| 7 |
Centro de Investigaciones Endocrinológicas "Dr. César Bergadá" (CEDIE) CONICET - FEI - División de Endocrinología, Hospital de Niños "Ricardo Gutiérrez", Ciudad Autónoma de Buenos Aires, Argentina. https://orcid.org/0000-0003-3864-8278 |
| 8 |
Instituto de Lactología Industrial (INLAIN, CONICET-UNL), Facultad de Ingeniería Química, Universidad Nacional del Litoral, Santa Fe, Argentina. https://orcid.org/0000-0002-6190-8528 |
Correspondencia: Gabriel Vinderola
E-mail: gvinde@fiq.unl.edu.ar
Presentado: 30/9/25. Aceptado: 16/12/25
RESUMEN
La fenilcetonuria (PKU) es una enfermedad genética que afecta el metabolismo de la fenilalanina. El tratamiento implica una dieta baja en fenilalanina, complementada con sustitutos proteicos y fórmulas infantiles. La lactancia materna, pese a su contenido de fenilalanina, es promovida por sus múltiples beneficios, siempre que sea controlada y combinada con fórmulas especiales. En este contexto, el desarrollo temprano y adecuado de la microbiota intestinal adquiere un rol relevante, ya que influye en la inmunidad, el metabolismo y el desarrollo neurológico. Sin embargo, los bebés con PKU pueden tener un perfil de microbiota alterado por el menor consumo de lactosa y oligosacáridos de leche humana, naturalmente presentes en la leche materna. Esto resalta la importancia de continuar adaptando las fórmulas y sustitutos proteicos para acercarse lo más posible a la composición de la leche humana, promoviendo así una microbiota saludable que contribuya al bienestar integral del niño con PKU. Esta revisión sintetiza la evidencia sobre microbiota intestinal, lactosa y abordaje nutricional en PKU pediátrica, analizando cómo la restricción de lactosa y de oligosacáridos de la leche humana y las estrategias de lactancia/fórmulas moldean la eubiosis y el control metabólico, y delineando implicancias clínicas y prioridades de investigación.
Palabras clave: fenilcetonuria, PKU, lactancia, lactosa, microbiota, fórmulas especiales.
ABSTRACT
Phenylketonuria (PKU) is a genetic disorder that affects phenylalanine metabolism. Treatment involves a low-phenylalanine diet, supplemented with protein substitutes and infant formulas. Breastfeeding, despite its phenylalanine content, is promoted for its many benefits, provided it is monitored and combined with special formulas. In this context, the early and adequate development of the gut microbiota plays an important role, as it influences immunity, metabolism, and neurological development. However, infants with PKU may have an altered microbiota profile due to lower consumption of lactose and human milk oligosaccharides, which are naturally present in breast milk. This highlights the importance of continuing to adapt formulas and protein substitutes to come as close as possible to the composition of human milk, thus promoting a healthy microbiota that contributes to the overall well-being of children with PKU. This review synthesizes the evidence on gut microbiota, lactose, and nutritional approaches in pediatric PKU, analyzing how lactose and human milk oligosaccharide restriction and breastfeeding/formula strategies shape eubiosis and metabolic control, and outlining clinical implications and research priorities.
Keywords: phenylketonuria, PKU, breastfeeding, lactose, microbiota, special formulas.
INTRODUCCIÓN
La fenilcetonuria (PKU), causada por la deficiencia de la enzima fenilalanina hidroxilasa, es uno de los errores congénitos del metabolismo (ECM) más prevalentes. Se trata de una enfermedad hereditaria autosómica recesiva que afecta al metabolismo de la fenilalanina, lo que conduce a hiperfenilalaninemia y, en ausencia de tratamiento, puede provocar daño neurológico. Sin intervención oportuna, puede evolucionar hacia manifestaciones severas, como discapacidad intelectual profunda, convulsiones y problemas conductuales1. El conocimiento acerca del microbioma intestinal ha arrojado nueva luz sobre enfermedades que desde hace tiempo se sabe que son multifactoriales. Aunque los ECM son enfermedades monogénicas, el genotipo por sí solo no es suficiente para explicar la gran variabilidad fenotípica observada. La alimentación influye sobre el microbioma, y una dieta especial se utiliza (sola o como coadyuvante) en el abordaje nutricional de numerosos ECM2. El objetivo de este trabajo fue revisar de forma narrativa la relación entre PKU, dieta, lactosa, microbioma y salud en individuos con PKU.
MÉTODOS
La metodología utilizada fue una revisión no sistemática del tipo narrativa sobre el diagnóstico y prevalencia de la fenilcetonuria (PKU), el abordaje nutricional actual, el rol de la microbiota en el desarrollo infantil, la composición de la microbiota en niños con PKU, el rol de la lactosa en la microbiota y el aporte de esta en la leche humana, fórmulas y sustitutos proteicos. Los autores utilizaron las bases de datos Scopus, ScienceDirect y PubMed, así como otras fuentes consideradas de interés. JS desarrolló la situación epidemiológica actual de la PKU, AB y MN desarrollaron el abordaje nutricional, VB y GV desarrollaron lo referente a microbiota intestinal, MGV y MS desarrollaron lo referente a lactosa e IB lo referente a prebióticos. Todos los autores revisaron y aprobaron la versión final del manuscrito.
RESULTADOS Y DISCUSIÓN
Fenilcetonuria: diagnóstico y prevalencia
El diagnóstico precoz se realiza a través de la pesquisa neonatal, y el inicio temprano de un tratamiento continuo permite preservar el desarrollo intelectual, aunque con una capacidad neurocognitiva ligeramente reducida en promedio. La dieta restringida en fenilalanina ha constituido la estrategia terapéutica principal durante más de 60 años, demostrando ser eficaz, aunque con dificultades en la adherencia1.
La prevalencia global de la PKU es de aproximadamente 1 cada 23.930 nacidos vivos, afectando a unas 450.000 personas mundialmente. La prevalencia varía significativamente entre regiones y grupos étnicos, con tasas más altas en Turquía (1:2.600), Italia (1:4.000) e Irlanda (1:4.500), y más bajas en Japón (1:125.000) y Tailandia (1:227.273)1. En Argentina, la prevalencia es de 1:15.715. Su expresión clínica también muestra variabilidad, con una distribución fenotípica global de 62 % PKU clásica, 22 % PKU leve y 16 % hiperfenilalaninemia leve. En algunos casos, la correlación entre genotipo y fenotipo permite predecir con precisión la gravedad de la enfermedad y la respuesta a tratamientos como la tetrahidrobiopterina, facilitando una terapia personalizada3.
Los programas de pesquisa neonatal son fundamentales para el diagnóstico precoz de la PKU. La cobertura es variable: Brasil implementó su programa en 2001, alcanzando una cobertura del 85,8 %; Argentina logró una cobertura del 90 % en 2006; mientras que, en México, la cobertura es regional y no está coordinada a nivel nacional, aunque supera el 70 %. En conjunto, 14 de los 20 países de América Latina han adoptado programas de pesquisa neonatal para la detección de PKU4,5. En la última década se ha observado un crecimiento sostenido y significativo, destacado por la implementación de nuevos programas, el aumento de la cobertura, la expansión del panel de enfermedades, la promulgación de nuevas leyes y la creciente participación de las autoridades gubernamentales y de salud pública4. Aunque se han logrado avances significativos en el diagnóstico y tratamiento de la PKU, persisten desafíos en la implementación uniforme de programas de pesquisa neonatal y en el acceso equitativo a terapias avanzadas, especialmente en regiones con recursos limitados. En este contexto, resulta esencial fortalecer las políticas de salud pública y la infraestructura médica para mejorar los resultados clínicos y la calidad de vida de los pacientes4.
Abordaje nutricional y lactancia en casos de PKU
El tratamiento vigente, seguro y eficaz es una dieta estricta, que consiste en una ingesta de proteínas naturales restringida, una mezcla de aminoácidos o sustituto proteico libre de fenilalanina para completar el requerimiento proteico y otros nutrientes esenciales y el aporte de alimentos muy bajos en proteínas para cubrir calorías y mantener los dosajes de fenilalanina en sangre en rangos adecuados, siendo este tratamiento de carácter permanente. Ante esta restricción, la lactancia materna estaría afectada6. Sin embargo, las guías europeas recomiendan el fomento de la lactancia, en lugar de utilizar fórmula de inicio (FI) como fuente de fenilalanina7. Para estos pacientes, entre otras ventajas de la leche humana8, se destacan: su bajo contenido en fenilalanina, presencia de ácido docosahexaenoico, lactosa, inmunoglobulinas, hierro altamente biodisponible, entre otros, y otorga beneficios emocionales relacionados con el vínculo entre madre y el hijo con una enfermedad crónica.
Existe evidencia robusta en relación con la lactancia en bebés PKU, lográndose niveles sanguíneos seguros de fenilalanina, alcanzando un adecuado crecimiento y desarrollo, siempre que se administre junto con un sustituto proteico (SP) sin o con bajo contenido de fenilalanina. La primera experiencia exitosa se describió en los años 809. A partir de allí, se han descrito numerosos trabajos8,10. Si bien hay diferentes maneras seguras de permitir lactancia en PKU11, en general, se indica un volumen determinado de SP, reduciendo la ingesta de leche humana, para lograr una ingesta adecuada de fenilalanina. Los cálculos para esta indicación dependen del peso del paciente, la tolerancia y el contenido de fenilalanina en la leche humana12. Para ello, se pueden utilizar planillas de cálculo específicas para PKU y también para otros ECM13.
Dado que los SP pueden representar una parte sustancial de la ingesta nutricional de los lactantes con PKU, es importante que su composición evolucione y se aproxime lo máximo posible a la composición de la leche humana8, aun sabiendo que la composición de una fórmula es estática, mientras que la de la leche humana cambia a lo largo de la lactancia14.
Rol de la microbiota en el desarrollo infantil
La microbiota intestinal desempeña un rol central en el desarrollo infantil, impactando en procesos fisiológicos, inmunológicos y neurobiológicos desde el nacimiento. Esta asociación emergente entre microbiota y desarrollo ofrece un enfoque innovador para la prevención en salud, constituyendo un pilar esencial de la medicina pediátrica. La composición y maduración del microbioma están influenciadas por factores como el tipo de parto, la alimentación (lactancia, fórmula o mixta, y la alimentación complementaria), la edad gestacional, la exposición a antibióticos, el entorno familiar y la convivencia con hermanos o mascotas. La colonización vaginal facilita la transferencia de microbiota materna beneficiosa, mientras que la cesárea se asocia con un perfil microbiano distinto que aumenta el riesgo de alergias y enfermedades respiratorias. La lactancia materna favorece la expansión de géneros beneficiosos como Bifidobacterium, en contraste con la fórmula. La exposición precoz a antibióticos disminuye la diversidad microbiana y se ha vinculado con mayor prevalencia de asma, obesidad y alergias15.
Desde el punto de vista somático, la microbiota intestinal regula la eficiencia en la obtención de energía, la señalización hormonal del crecimiento y la respuesta inmunológica. La mayor producción de ácidos grasos de cadena corta, como el butirato, con propiedades antiinflamatorias e inmunomoduladoras, induce la proliferación de células T reguladoras en el colon, estimula la liberación de citocinas antiinflamatorias y previene la inflamación intestinal, disminuyendo así el riesgo de enfermedades autoinmunes, inflamatorias y alérgicas16.
El eje intestino-cerebro constituye una vía de comunicación bidireccional regulada por el sistema nervioso y la microbiota, que produce neurotransmisores como serotonina, dopamina y GABA. La microglía, célula inmunitaria residente del sistema nervioso central, cumple funciones clave en la poda sináptica y en la respuesta neuroinmune, las cuales pueden verse alteradas por la disbiosis. Esta condición compromete la barrera hematoencefálica y la señalización neuronal17.
Microbiota intestinal en población PKU
Se ha reportado la condición de la microbiota intestinal en individuos PKU, y el efecto de la dieta en la misma. En niños de1 a 8 años, se reportó menor diversidad de la microbiota, una menor concentración de Bifidobacterium y aumento de proteobacterias, conocidas por su capacidad inflamatoria18. En niños de 2 a 8 años, se detectó menor diversidad y menor presencia de bacterias anaerobias estrictas productoras de butirato19. Una menor diversidad se confirmó también en trabajos en adultos con PKU20,21. Por su parte, dos estudios en niños de 4 a 12 años y en niños de 5 a 13 años con PKU demostraron efectos desfavorables en la microbiota al implementar la dieta específica, relacionados a una menor concentración de bacterias productoras de butirato23,24. Las restricciones dietarias llevadas a cabo en niños de 1 a 11 años también demostraron un impacto negativo en la diversidad de la microbiota oral e intestinal25. En cuanto a la diversidad microbiana, los trabajos referidos la analizan mediante secuenciación parcial del gen ARNr 16S para el estudio de bacterias, o mediante metagenómica (shotgun), que permite evaluar bacterias, levaduras, hongos, virus, arqueas y protozoarios. La diversidad alfa describe la diversidad dentro de una misma muestra (riqueza y equidad de abundancias); los índices más usados incluyen OTUs/ASVs observados, Chao1, Shannon, Simpson y la diversidad filogenética de Faith. La diversidad beta evalúa las diferencias entre muestras o grupos; se emplean, entre otros, Bray-Curtis, Jaccard y UniFrac (ponderada y no ponderada).
Lactosa en lactancia, fórmulas de inicio y sustitutos proteicos para PKU
La leche humana contiene entre 60 y 80 g/L de lactosa, manteniéndose en ese rango hasta al menos los dos años de lactancia26. Durante el primer año, los lactantes consumen entre 30 y 72 g de lactosa/día26. Parte de esta lactosa llega al colon, favoreciendo el crecimiento de bifidobacterias mediante adaptación colónica27. Se comparó la ingesta de lactosa entre lactantes sin PKU alimentados exclusivamente con leche humana o fórmula de inicio, y lactantes con PKU alimentados con leche humana, fórmula de inicio y sustitutos proteicos con distintos contenidos de lactosa (SP A: 1,7 %; SP B: 33 %). El análisis incluyó escenarios con baja tolerancia a la fenilalanina (130 mg) al mes y a los 6 meses de vida12,28,29. En Argentina también existen SP sin lactosa (Tabla 1 y 2).
| Tabla 1: Ingesta diaria de lactosa vía leche humana (LH) en los primeros seis meses de vida
|
| |
 |
| |
| a Se estiman 7,2 gramos de lactosa en 100 ml de leche humana (rango 6,7-7,8 % p/v). Tabla elaborada con datos publicados12,28. |
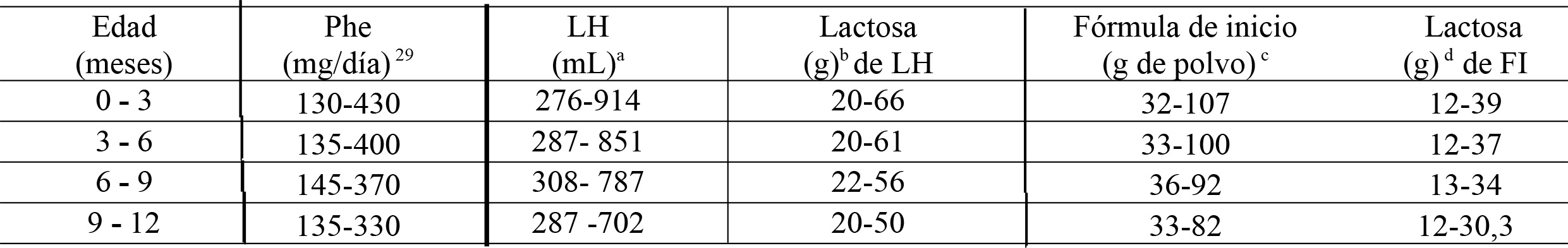
| Tabla 2: Ingesta estimada de lactosa en lactantes PKU, alimentados con leche humana o formula de inicio, según tolerancia de Phe
|
| |
 |
| |
a Se consideran 47 mg de Phe en 100 ml de leche humana29.
b Se consideran 7,2 (promedio 6,7-7,8 gr%) g de lactosa en 100 ml de leche humana30.
c Se consideran 60 mg de Phe en 100 ml de fórmula de inicio dilución 15%29.
d Se consideran 37 gr de lactosa promedio, en 100 gr de polvo de FI (información promedio según lo declarado en el rótulo de composición química, entre cinco fórmulas de inicio comerciales disponibles en Argentina que variaban entre 27-47mg lactosa %).
|
Durante el primer año de vida, los lactantes PKU con baja tolerancia a la fenilalanina consumirían menos lactosa que aquellos alimentados exclusivamente con leche humana. Solo a los 30 días, aquellos con alta tolerancia (430 mg Phe) pueden superar esa ingesta (66 g vs. 50 g) (Tabla 3).
| Tabla 3: Análisis comparativo de la ingesta de lactosa en lactantes PKU al mes y a los 6 meses de vida con lactancia humana, fórmula de Inicio (FI) y los sustitutos proteicos A y B
|
| |
 |
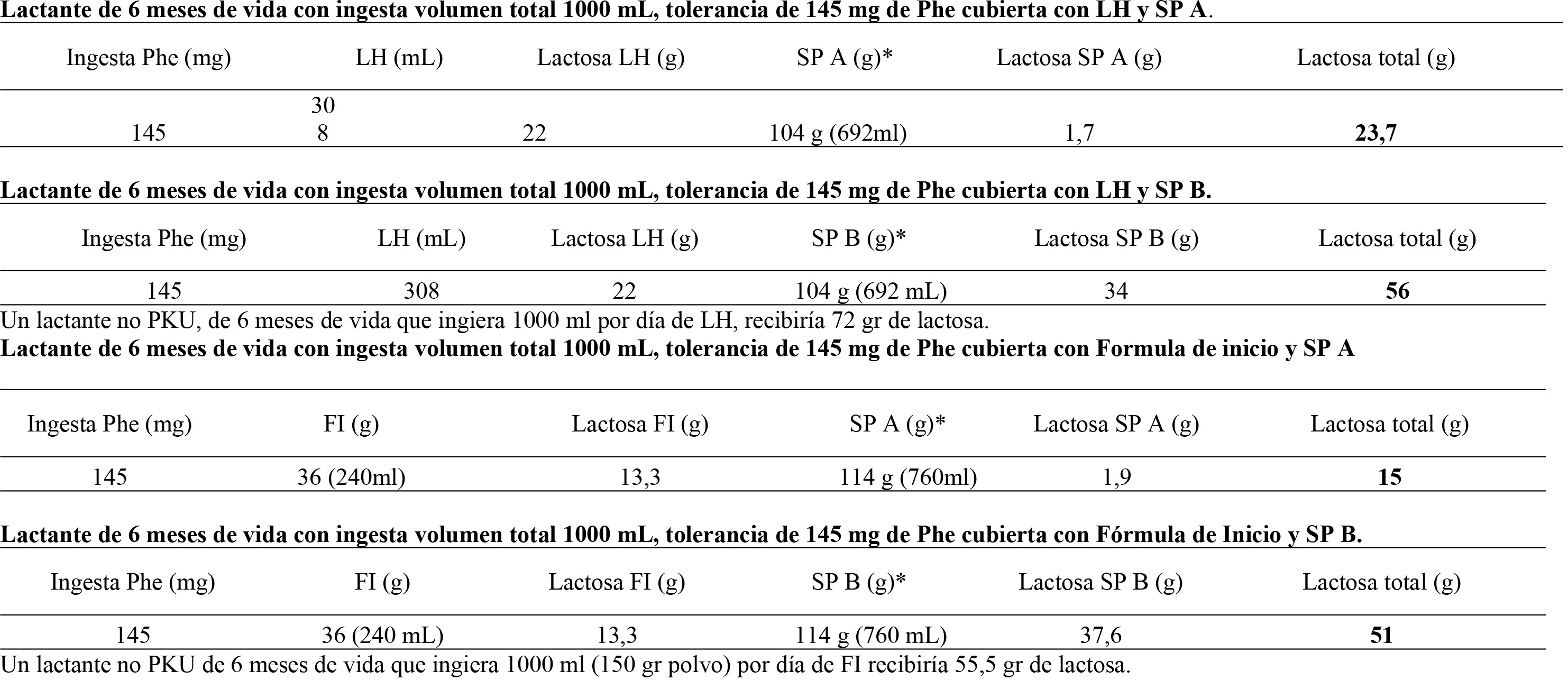
Por ejemplo, un bebé de 1 mes de vida sin PKU consume 50 g de lactosa en 700 mL de leche humana, mientras que un lactante con PKU recibe entre 12 y 41 g. Un bebé de 6 meses sin PKU consume 72 g de lactosa diariamente, mientras que un bebé PKU recibe entre 13 y 56 g de lactosa. En ambos casos, la cantidad ingerida de este disacárido dependerá de la cantidad de leche humana, fórmula de inicio y tipo de sustituto proteico utilizados (Tabla 4).
| Tabla 4: Análisis comparativo de la ingesta de lactosa en lactantes PKU al mes y a los 6 meses de vida con lactancia humana, fórmula de Inicio (FI) y los sustitutos proteicos A y B (continuación)
|
| |
 |
| |
| * Sustituto proteico A, para menores de 1 año, contiene 1,7 gr de lactosa en 100 gr de polvo. ** Sustituto proteico B para menores de 1 año, contiene 33 gr de lactosa en 100 gr de polvo. *** Se consideran 60 mg de Phe en 100 ml de Formula de Inicio (FI) con una dilución del 15%, es decir en 15 gr de polvo de FI, 60 mg Phe, ****Se consideran 37 gr de lactosa en 100 gr de polvo de FI |
A lo largo del primer año, los lactantes con PKU consumen menos lactosa que los no PKU. En Argentina, los SP disponibles a partir del primer año de vida, no contienen lactosa, a excepción de los glicomacropéptidos (GMP) que sí la contienen (GMP en polvo: entre 0,05 g y 0,36 g % y GMP líquido menos de 0,5 g por porción de 250 ml).
Prebióticos en fórmulas para pacientes PKU
Oligosacáridos con efecto prebiótico como los Galactooligosacáridos (GOS) y Fructooligosacáridos (FOS) se han incorporado en fórmulas infantiles para PKU, con un aporte de 0,8 g/100 mL de una combinación de GOS (90 %) y FOS (10 %)31. Numerosos estudios confirman la eficacia y seguridad de los prebióticos sobre la salud del lactante en relación a la modulación del sistema inmune, a favorecer la proliferación de bifidobacterias y a una menor prevalencia de atopia. En relación a su acción metabólica, por fermentación colónica se produce butirato. Nutricionalmente, estimulan la síntesis de vitaminas B6, B12, ácido fólico, ácido nicotínico, así como la absorción de calcio, magnesio, hierro y zinc, además de disminuir la incidencia de infecciones intestinales y respiratorias31. El conocimiento sobre la función gastrointestinal y los hábitos intestinales de los bebés con trastornos de aminoácidos es limitado, aunque se destacan problemas de estreñimiento, diarrea y disconfort abdominal, posiblemente asociados a una alta ingesta de sustitutos proteicos de alta osmolaridad. Si bien estos efectos por sí solos son indeseables, la función intestinal anormal puede alterar la alimentación, que, en última instancia, afecta al control metabólico. Comprender la influencia de los moduladores intestinales, contribuiría a mejorar la alimentación y a obtener beneficios para estos pacientes32. Dado que los lactantes PKU reciben lactancia restringida, la falta de los oligosacáridos normalmente presentes en la leche materna podría estar asociada con un aumento del pH fecal y una reducción de bifidobacterias, predisponiendo al paciente a trastornos gastrointestinales y otras afecciones22,23. Los sustitutos proteicos que contienen prebióticos (scGOS/ lcFOS [relación 9:1]) estabilizan y favorecen un microbioma intestinal más cercano a la de los bebés amamantados, con niveles de bifidobacterias adecuados y pH fecal bajo, brindando beneficios para su salud, como un sistema de defensa eficaz contra las infecciones y un mejor control metabólico22.
CONCLUSIONES
La fenilcetonuria es un trastorno metabólico cuya detección precoz y tratamiento dietético estricto permite un desarrollo neurológico adecuado. En Argentina es una enfermedad de pesquisa obligatoria. La lactancia materna es segura y beneficiosa en casos de PKU si se ajusta la ingesta de fenilalanina, promoviendo efectos positivos sobre el vínculo madre-hijo y el desarrollo intestinal. El desarrollo de la microbiota es esencial para el desarrollo infantil integral. En los casos de PKU, la microbiota presenta menos diversidad y abundancia de géneros benéficos como Bifidobacterium y aumento de grupos microbianos inflamatarios como proteobacterias La ingesta de lactosa y prebióticos en pacientes PKU suele ser menor, lo que podría comprometer su microbiota, inmunidad y neurodesarrollo. Teniendo en cuenta los efectos benéficos de la lactosa en la configuración de la microbiota intestinal y sus funciones, y por lo expuesto, se sugiere considerar la necesidad de implementar medidas para equiparar la ingesta de lactosa de pacientes PKU con aquellos no PKU que reciben lactancia exclusiva. Sería importante revisar el contenido de lactosa de los sustitutos proteicos y promover la lactancia materna, indicando la mayor cantidad de leche humana posible, manteniendo la ingesta de fenilalanina en rangos seguros. Asimismo, podría contemplarse el uso de prebióticos (p. ej., mezclas tipo scGOS/lcFOS o alimentos médicos a base de GMP) como estrategia adyuvante para favorecer perfiles microbianos beneficiosos, reconociendo que la evidencia clínica específica en PKU aún es limitada. Es necesario continuar trabajando en la mejora composicional de sustitutos proteicos y fórmulas infantiles para contribuir al desarrollo y calidad de vida de individuos con PKU.
Financiamiento
Danone Specialized Nutrition (DSN) facilitó los encuentros para la organización del trabajo mediante plataformas digitales y cubrió los honorarios profesionales del tiempo requerido para la redacción de este artículo, sin tener injerencia en los contenidos ni en la versión final del artículo.
Conflictos de interés
Jacqueline Schuldbeg es Medical Manager de Epilepsia & Errores Congénitos del Metabolismo en DSN, el resto de los autores declaran que su única relación con DSN fue haber participado como disertantes en conferencias o simposios organizados por la empresa. GV es miembro del cuerpo de directores científicos de la International Scientific Association of Probiotics and Prebiotics (ISAPP).
REFERENCIAS
- Van Spronsen FJ, Blau N, Harding C, Burlina A, Longo N, Bosch AM. Phenylketonuria. Nat Rev Dis Primers. 2021 May 20;7(1):36.
- Colonetti K, Roesch LF, Schwartz IVD. The microbiome and inborn errors of metabolism: Why we should look carefully at their interplay? Genet Mol Biol. 2018 Jul/Sept.;41(3):515-532.
- Hillert A, Anikster Y, Belanger-Quintana A, Burlina A, Burton BK, Carducci C, et al. The Genetic Landscape and Epidemiology of Phenylketonuria. Am J Hum Genet. 2020 Aug 6;107(2):234-250.
- Chiesa A, Spécola N, Poubel M, Vela-Amieva M, Jurecki E, Vilela DR, et al. Adherence to PKU guidelines among patients with phenylketonuria: A cross-sectional national multicenter survey-based study in Argentina, Brazil, and Mexico. Mol Genet Metab Rep. 2023 Nov 21;38:101026.
- Borrajo GJC. Newborn screening in Latin America: A brief overview of the state of the art. Am J Med Genet C Semin Med Genet. 2021; 187(3): 322-328.
- MacDonald A, van Wegberg AMJ, Ahring K, Beblo S, Bélanger-Quintana A, Burlina A, et al. PKU dietary handbook to accompany PKU guidelines. Orphanet J Rare Dis. 2020 Jun 30;15(1):171.
- van Wegberg AMJ, MacDonald A, Ahring K, Bélanger-Quintana A, Blau N, Bosch AM, et al. The complete European guidelines on phenylketonuria: diagnosis and treatment. Orphanet J Rare Dis. 2017 Oct 12;12(1):162.
- Ilgaz F, Höller A, Marsaux C, Banta-Wright S, Coşkun T, Dingess KA, et al. Human Milk Feeding in Inherited Metabolic Disorders: A Systematic Review of Growth, Metabolic Control, and Neurodevelopment Outcomes. J Inherit Metab Dis. 2025 Mar;48(2):e70001.
- Francis DEM, Smith I. Breast-feeding regime for the treatment of infants with phenylketonuria. In Bateman C, ed. Applied Nutrition. London: John Libbey; 1981: 82–83.
- Kalvala J, Chong L, Chadborn N, Ojha S. Breast feeding in infants diagnosed with phenylketonuria (PKU): a scoping review. BMJ Paediatr Open. 2023 Oct;7(1):e002066.
- Zuvadelli J, Paci S, Salvatici E, Giorgetti F, Cefalo G, Re Dionigi A, Rovelli V, et al. Breastfeeding in Phenylketonuria: Changing Modalities, Changing Perspectives. Nutrients. 2022 Oct 5;14(19):4138.
- Greve LC, Wheeler MD, Green-Burgeson DK, Zorn EM. Breast-feeding in the management of the newborn with phenylketonuria: a practical approach to dietary therapy. J Am Diet Assoc. 1994 Mar;94(3):305-9.
- Vitoria-Miñana I, Couce M L, González-Lamuño D, García-Peris M, Correcher-Medina P. Breastfeeding and Inborn Errors of Amino Acid and Protein Metabolism: A Spreadsheet to Calculate Optimal Intake of Human Milk and Disease-Specific Formulas. Nutrients, 2023;15(16): 3566.
- Plows JF, Berger PK, Jones RB, Alderete TL, Yonemitsu C, Najera JA, et al. Longitudinal Changes in Human Milk Oligosaccharides (HMOs) Over the Course of 24 Months of Lactation. J Nutr. 2021 Apr 8;151(4):876-882.
- Robertson RC, Manges AR, Finlay BB, Prendergast AJ. The Human Microbiome and Child Growth - First 1000 Days and Beyond. Trends Microbiol. 2019 Feb;27(2):131-147.
- Dugas LR, Lie L, Plange-Rhule J, Bedu-Addo K, Bovet P, Lambert EV, et al. Gut microbiota, short chain fatty acids, and obesity across the epidemiologic transition: the METS-Microbiome study protocol. BMC Public Health. 2018 Aug 6;18(1):978.
- Agustí A, García-Pardo MP, López-Almela I, Campillo I, Maes M, Romaní-Pérez M, et al. Interplay Between the Gut-Brain Axis, Obesity and Cognitive Function. Front Neurosci. 2018 Mar 16;12:155
- Su Y, Shadike Q, Wang M, Jiang H, Liu W, Liu J, Tuerdi R, et al. A low abundance of genus Bacteroides in gut microbiota is negatively correlated with blood phenylalanine levels in Uygur patients with phenylketonuria. Transl Pediatr. 2021 Oct;10(10):2521-2532.
- Pinheiro de Oliveira F, Mendes RH, Dobbler PT, Mai V, Pylro VS, Waugh SG, et al.. Phenylketonuria and Gut Microbiota: A Controlled Study Based on Next-Generation Sequencing. PLoS One. 2016 Jun 23;11(6):e0157513.
- Mancilla VJ, Mann AE, Zhang Y, Allen MS. The Adult Phenylketonuria (PKU) Gut Microbiome. Microorganisms. 2021 Mar 4;9(3):530.
- Timmer C, Davids M, Nieuwdorp M, Levels JHM, Langendonk JG, Breederveld M, et al. Differences in faecal microbiome composition between adult patients with UCD and PKU and healthy control subjects. Mol Genet Metab Rep. 2021 Sep 8;29:100794
- Verduci E, Carbone MT, Borghi E, Ottaviano E, Burlina A, Biasucci G. Nutrition, Microbiota and Role of Gut-Brain Axis in Subjects with Phenylketonuria (PKU): A Review. Nutrients. 2020 Oct 29;12(11):3319
- Verduci E, Moretti F, Bassanini G, Banderali G, Rovelli V, Casiraghi MC, et al. Phenylketonuric diet negatively impacts on butyrate production. Nutr Metab Cardiovasc Dis. 2018 Apr;28(4):385-392.
- Bassanini G, Ceccarani C, Borgo F, Severgnini M, Rovelli V, Morace G, et al. Phenylketonuria Diet Promotes Shifts in Firmicutes Populations. Front Cell Infect Microbiol. 2019 Apr 16;9:101.
- Ostrowska M, Nowosad K, Mikoluc B, Szczerba H, Komon-Janczara E. Changes in the Gut and Oral Microbiome in Children with Phenylketonuria in the Context of Dietary Restrictions-A Preliminary Study. Nutrients. 2024 Nov 16;16(22):3915.
- Siziba LP, Mank M, Stahl B, Gonsalves J, Blijenberg B, Rothenbacher D, et al. Human Milk Oligosaccharide Profiles over 12 Months of Lactation: The Ulm SPATZ Health Study. Nutrients. 2021 Jun 8;13(6):1973.
- Rios-Leyvraz M, Yao Q. The Volume of Breast Milk Intake in Infants and Young Children: A Systematic Review and Meta-Analysis. Breastfeed Med. 2023 Mar;18(3):188-197.
- Ojo-Okunola A, Cacciatore S, Nicol MP, du Toit E. The Determinants of the Human Milk Metabolome and Its Role in Infant Health. Metabolites. 2020; 10(2):77. https://doi.org/10.3390/metabo10020077
- Bernstein L, Rohr F, van Calcar S. Nutrition Management of Inherited Metabolic Diseases. Lessons from Metabolic University. 2nd ed. New York: Springer; 2022.
- Ballard O, Morrow AL. Human milk composition: nutrients and bioactive factors. Pediatr Clin North Am. 2013; 60(1):49-74.
- Vitoria Miñana I. Oligosacáridos en la Nutrición Infantil: fórmulas infantiles, alimentación complementaria y del adolescente. Acta Pediatr Esp. 2007; 65(4):175-179.
- MacDonald A, Cochrane B, Wopereis H, Loveridge N. Specific prebiotics in a formula for infants with Phenylketonuria. Mol Genet Metab. 2011;104 Suppl:S55-9.
|
|

